在如今,最火热的药物当属GLP-1,它已经成为名副其实的“药王”。由于社会快速发展,心血管疾病、糖尿病、肥胖这些与代谢相关的慢病出现了快速上升,而GLP-1靶点的代表,司美格鲁肽、替尔泊肽开始被大众所熟知。在药理学,药物的靶点是指药物作用的特定分子或受体,它们共同协调发挥治疗作用。单靶点、双靶点、三靶点则分别表示药物作用于一个、两个、三个不同的靶点。在GLP-1靶点中,单靶点、双靶点药物都有哪些区别?本文一文讲清。▍单靶点GLP-1
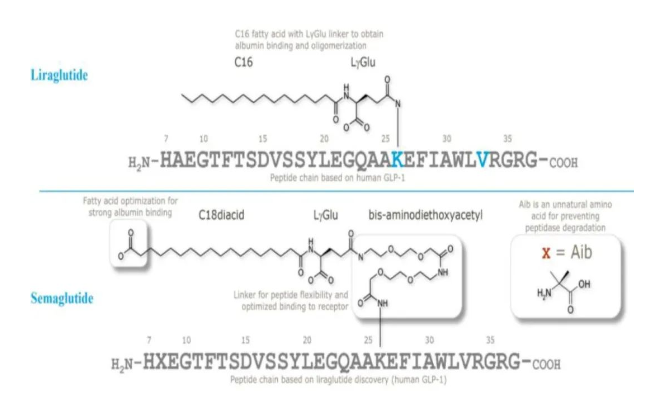
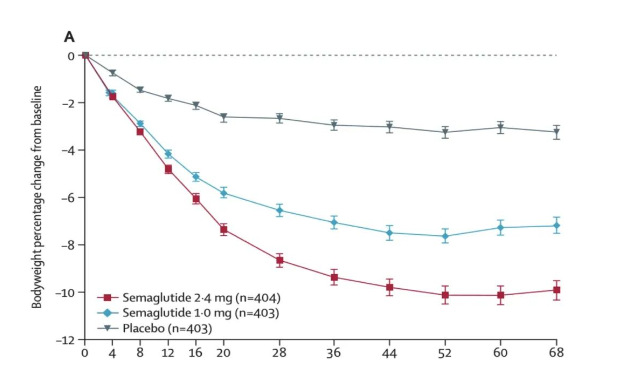
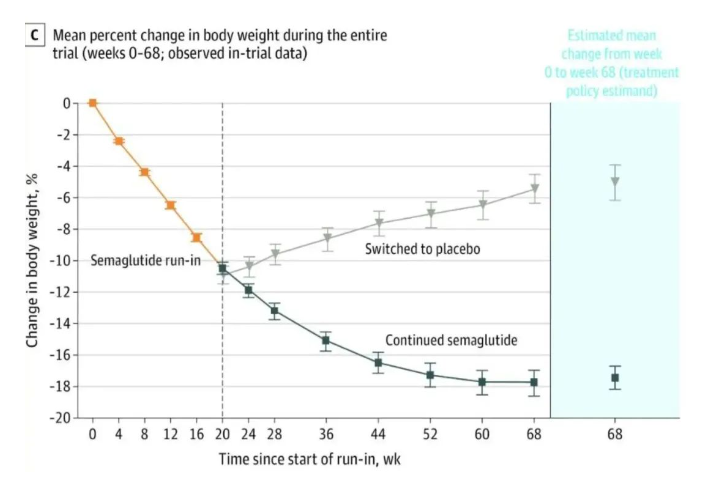
单靶点GLP-1药物是指只作用于GLP-1受体的药物,通过模拟或增强GLP-1的生物性来发挥作用。其可以促进胰岛素分泌、抑制胰高血糖素的释放以及减慢胃肠蠕动的速度,从而帮助降低血糖水平,治疗糖尿病,减缓胃排空,实现减重效果。其具体作用机制如下:1. 促进胰岛素分泌:胰岛素是调节血糖水平的重要激素,通过促进葡萄糖的向内运送和利用,使血糖水平降低。2. 抑制胰高血糖素分泌:胰高血糖素是胰细胞外的激素,具有提高血糖浓度的作用,GLP-1的作用可以使血糖升高的效应减弱。3. 减慢胃肠蠕动:抑制胃肠道运动,延缓胃肠蠕动的速度,从而使食物在消化道中停留的时间延长。这种作用有利于使饭后血糖升高的速度减慢,维护血糖的稳定。司美格鲁肽最初基于利拉鲁肽的长效替代面世,是单靶点药物。在第26位Lys(赖氨酸)上增加了两个羟乙基乙二胺,同时十六烷酰基脂肪酸换成十八烷酰基脂肪二酸, 进一步提高与白蛋白结合力。此外,8号位Ala(丙氨酸)被Aib(2-氨基异丁酸)取代,可以抵抗二肽基肽IV(DPP-4)的降解作用,半衰期延长至一周,可长效控制血糖及体重,同时在心血管、抗癌以及缓解阿尔兹海默症等领域具有潜在多重获益。司美格鲁肽最早于2017年获FDA批准用于II型糖尿病,2021年通过NMPA批准上市,并于2021、2022 年分获FDA、EMA批准用于成人超重及肥胖症。此外口服司美格鲁肽于2019年获FDA批准用于II型糖尿病,为全球第一个也是目前唯一一个获批上市的口服GLP-1RA药物(日制剂)。2022年被FDA批准扩展适应人群至12周岁以上。在患有超重或肥胖和2型糖尿病的成人中,与安慰剂相比,司美格鲁肽 2.4mg 每周一次注射可显著减轻体重。在纳入1210名患者(2.4mg组404人,1.0mg组403人)的step2研究中,与安慰剂组相比,每周一次皮下注射司美格鲁肽2.4mg可使患者体重降低9.7kg(-9.6%);而每周一次注射1.0mg 司美格鲁肽则使得体重减轻6.99%,减重效果优于对照组(降低3.42%)。在另一项针对不患有2型糖尿病的肥胖或超重患者的step4研究中,维持皮下司美格鲁肽2.4mg注射可以使体重持续减轻。该研究分为两个阶段,前20周为导入期,803名参与者完成注射,平均体重减轻10.6%。在20-68周,每周一次皮下注射司美格鲁肽2.4mg的患者体重持续下降,到68周的主要终点时,相较基线体重减轻17.4%。其中88.7%的患者体重下降5%或更多,79.0%的患者体重下降超过10%。▍双靶点GLP-1
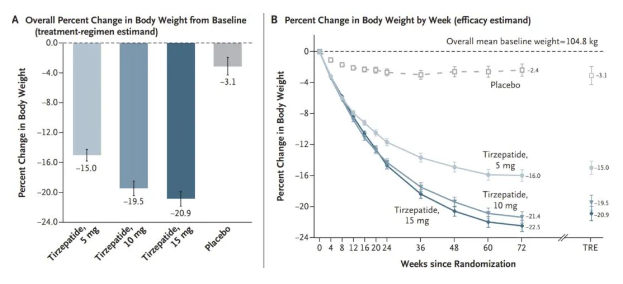
双靶点GLP-1药物是指同时作用于GLP-1受体和另一个靶点的药物。双靶点以GLP-1R/GIPR和GLP-1R/GCGR两类为主,前者国外已有上市产品,国内多处于1期或临床前阶段。后者国外最快3期,国内多处于1期跟随阶段。GLP-1R/FGF21R国内外进度相当,均处于1期研究阶段。双靶点GLP-1药物通过作用于多个靶点,协同发挥降血糖、降压、减脂、改善代谢的作用,同时疗效更全面,不同组合通过作用于不相同的生物过程发挥不一样的药理效应,在个性化糖尿病治疗中具有重要的地位。GIP(Glucose-dependent insulinotropic polypeptide,葡萄糖依赖性促胰岛素释放多肽)是第一个被发现的肠促胰素。在正常人体中,肠促胰素效应刺激的胰岛素分泌,约占整体胰岛素分泌总量的70%,其中GIP对整个肠促胰素效应的贡献占2/3,比重高于GLP-1。在血糖升高与GIP协同下,GIP可提高β细胞内环磷酸腺苷水平,呈葡萄糖依赖性促进β细胞的胰岛素分泌。因此,GIP受体激动剂是降糖疗法的重要补充。现已有多家制药企业开发研究GIP/GLP-1双受体激动剂。替尔泊肽(tirzepatide)是礼来公司研发并成功上市的一种GLP-1/GIP双受体激动剂,同样使用脂肪酸酰化修饰延长其半衰期。替尔泊肽可以说开启了降糖减重药物GLP-1/GIP的双靶点时代。替尔泊肽是一种含有 39 个氨基酸的合成线性肽分子,可同时激活 GLP-1和GIP受体。其将2种促胰岛素的作用整合至一个单分子中,从而达到高效控制血糖和体重的作用。替尔泊肽的肽序列包含两个非编码氨基酸残基(Aib,α-氨基异丁酸),位于第2位和第13位,这些残基导致其半衰期长,对白蛋白具有高亲和力,只需每周一次进行皮下注射 。替尔泊肽由礼来研发,于2022年5月获FDA批准,用于2型糖尿病治疗,9月分别获EMA及PMDA批准。2023年11月,替尔泊肽获FDA批准,用于超重肥胖人群。替尔泊肽是目前最早也是唯一一款获批上市的双靶点降糖药物,上市后销售爬坡速度远超度拉糖肽, 未来市场空间广阔。2022年5月礼来公布SURMOUNT-1研究达到两个共同主要终点,所有剂量均优于安慰剂。2539名肥胖且患有至少一种体重并发症(不包括糖 尿病)的成年志愿者在接受72周治疗后,5mg、10mg、15mg替尔泊肽实验组体重分别降低-15%、-19.5%、-20.9% 。2023年4月27日,礼来公布替尔泊肽针对肥胖症的 III 期临床 SURMOUNT-02 达到所有主要和次要终点,减重效果亮眼。对于肥胖或超重且患有2型糖尿病的成年人,15mg 替尔泊肽在 72 周实现15.7%的减重效果,即在基线 100.7 kg的体重下减重15.6 kg。与安慰剂相比,10mg和15mg的替尔泊肽都显著降低了体重。10mg、15mg 组分别有81.6%和 86.4%的患者减重5%以上,41.4%和51.8%的患者体重降低15%以上,而安慰剂组比例为30.6%和2.6%。GCG(Glucagon,胰高糖素)是由胰岛α细胞分泌,能够抑制胰岛素分泌并促进肝糖原分解从而升高血糖的一种激素。激动GCG受体造成的升糖作用,可以被激动GLP-1受体带来的葡萄糖浓度依赖性促胰岛素分泌作用和抑制胰高糖素分泌作用所对抗;而激动GCG受体带来的能量分解作用,与激动GLP-1受体带来的减少进食作用可协同降低体重。由于GCG与GLP-1氨基酸序列高度同源,因此在双受体激动剂研发上具有高度可行性。▍三靶点GLP-1
三靶点GLP-1是指同时作用于GLP-1受体、另一个糖尿病相关的受体以及另一个治疗糖尿病的作用靶点的药物或治疗策略。鉴于GLP-1、GCG、GIP的代谢调控作用,且相互之间具有鲜明的协同作用,因此多个医药公司也开始研发GLP-1/GCG/GIP三受体激动剂。Retatrutide是礼来公司研发的一种39个氨基酸且经脂肪酸酰化修饰的长效多肽,由GIP肽骨架设计而成,可在GCG、GIP和GLP-1受体上实现三重激动剂活性,可以通过增加能量消耗和减少热量摄入来减轻体重。Retatrutide在健康受试者中的安全性和耐受性与其他基于肠促胰素疗法相似。在一项Ⅱ期临床研究中,retatrutide(1 mg、4 mg、8 mg 或 12 mg)治疗24周时,肥胖或超重(糖尿病除外)成人患者平均减重17.5%,以最高剂量每周12 mg帮助成人肥胖患者在48周内平均减重24%。GLP-1三靶点药物的优势在于通过多重目标的作用,同时调节胰岛素分泌、胰高血糖抑制、胃肠蠕动、肾脏代谢和脂代谢等方面,到更全面的治疗效果。然而,这些药物的应用需要一步的研究和临床实践来证实其有效性和安全性。▍附:在研重磅GLP-1药物
玛仕度肽:全球首个进入注册临床的GLP-1/GCGR双靶点玛仕度肽(Mazdutide,IBI362)是由信达与礼来共同推进的一种哺乳动物胃泌酸调节素(OXM3)类似的长效合成肽。其利用脂肪酰基侧链延长作用时间 , 允许每周给药一次。可通过激动GLP-1R促进胰岛素分泌,发挥降糖减重功效,此外,还可通过激动 GCGR增加能量消耗增强减重疗效,并改善肝脏脂肪代谢。AMG133:潜在“first-in-class”双特异性抗体多肽偶联物
AMG133与替尔泊肽同样作用于GLP-1R和GIPR双靶点,但作用机制相反。AMG133是安进开发的一款潜在“first-in-class”双特异性抗体多肽偶联物(GIPR抗体偶联GLP-1),将GLP-1类似物通过18肽linker化学偶联到GIPR抗体重链上,可激活 GLP-1R 并抑制 GIPR(与替尔泊肽 GLP-1R/GIPR双重激动相反)。AMG133给药频率更低,疗效优秀。根据安进2022年12月公布的I期临床数据,经过85天治疗(每4周给药一次,共12周),140mg低剂量组、 420mg高剂量组的受试者体重平均降低7.19%、14.52%,效果显著优于安慰剂组(+1.49%)。目前II期临床试验已启动。Retatrutide:率先开启GLP-1三靶点III期减重临床
Retatrutide靶向GLP-1R/GIPR/GCGR。Retatrutide是一种含39个氨基酸的单肽,由GIP肽骨架设计而成,可在GCGR、GIPR和GLP-1R上实现三重激动剂活性,人体内平均半衰期长达6天。减重效果具有优于替尔泊肽的潜力。针对不伴有2型糖尿病的肥胖患者II期临床结果表明,接受48周Retatrutide后,最高剂量组患者体重降低22- 24%,主要受益于脂肪含量的减少,针对含有2型糖尿病患者,接受36周Retatrutide后,最高剂量组Hb1A降低2%,体重减轻15-17%。2023年5 月31日,Retatrutide率先启动全球III期减重临床(TRIUMPH-3),计划入组1800例患者,为期113周研究,预计2026年完成。BI 456906是从天然肠道激素胃泌酸调节素中提取的每周皮下注射1次长效GLP-1R/GCGR双重激动剂。据Zealand Pharma此前披露,BI 456906对GLP-1R的亲和力是对GCGR的8倍。
美国食品药品监督管理局(FDA)批准礼来公司每周一次的双重GIP和GLP-1受体激动剂Mounjaro/zepbound(Tirzepatide,替西帕肽)注射液,作为饮食和运动的辅助疗法,以改善二型糖尿病成人的血糖控制及体重管理。好消息是全球首访物美价廉的替西帕肽已经上市!
更多相关替西帕肽相关知识,请联系微信:799887580或306248824或者2573909181。联系QQ:799887580或306248824